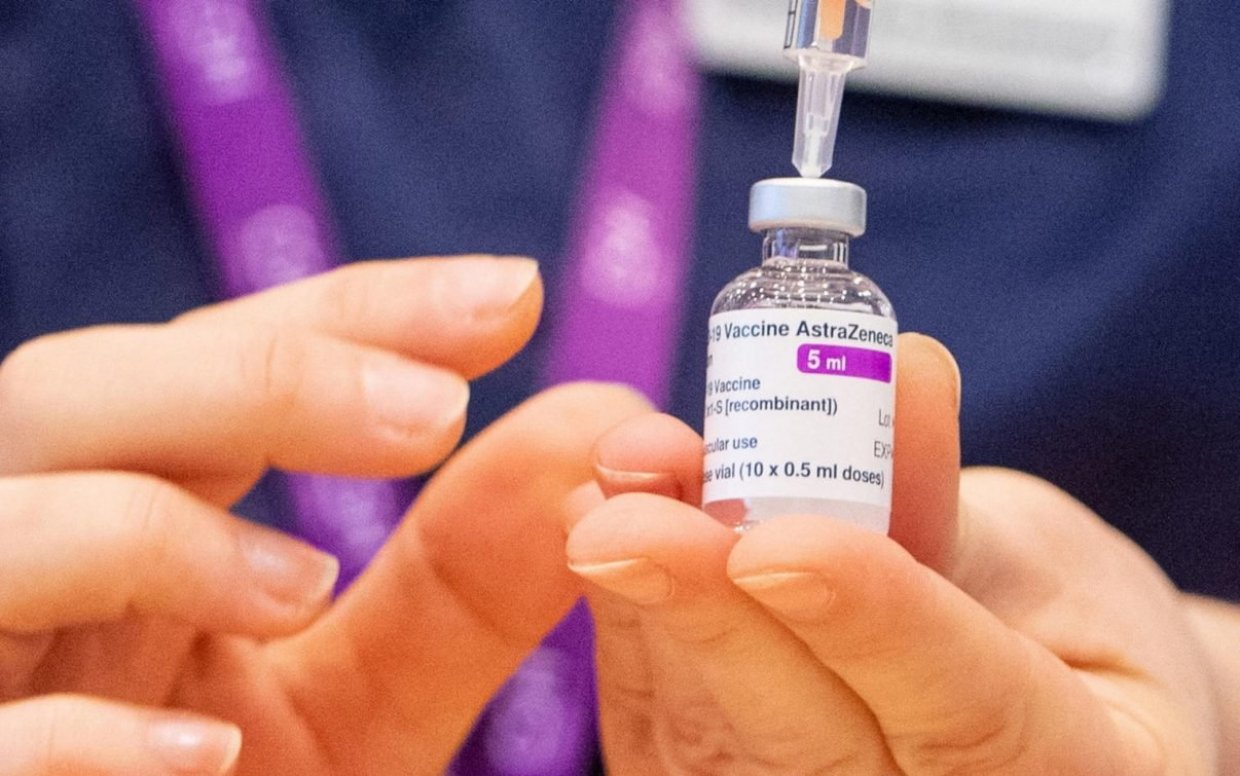
Ritirato il vaccino Astrazeneca
Ma...che ne è stato di Reithera?
10 maggio 2024 - E' di questi giorni la notizia che l’azienda anglo-svedese AstraZeneca ha ritirato il suo vaccino. Ricorderete anche che fu il primo ad avere una primissima sospensione temporanea ad inizio pandemia, poi però fu un coro: ''è sicuro'' lo dicevano Draghi, il Ministro della Salute e il team BuBa, virologi da salotto Burioni & Bassetti.
A fine aprile 2024 l'azienda aveva ammesso per la prima volta in documenti giudiziari, nel corso di un procedimento legale a Londra, che il suo vaccino anti Covid poteva causare trombosi come raro effetto collaterale. L’ammissione ora potrebbe aprire la strada a risarcimenti multimilionari, secondo i media britannici.
Ma a questo punto, cosa sappiamo esattamente riguardo agli altri prodotti anti-Covid: sono sicuri? E il mare di bugie che servivano a tenere viva la narrazione del vaccino come unica salvezza dal virus scappato dal mercato cinese di Wuhan?
Ma c'è un'altra domanda che ci riguarda da vicino: che ne è stato di Reithera? Lo ricordate?
Era il siero italiano – una profilassi classica, a ’vettore virale’, come AstraZeneca, Johnson&Johnson e Sputnik V – travolto dalla scelta europea di privilegiare i più tecnologici e moderni vaccini a RNA messaggero.
Fu finanziato con 12 milioni di euro di risorse dell’azienda, 8 milioni della Regione Lazio e poi con 81 milioni di euro dello Stato, forniti da Invitalia: 41,2 milioni a fondo perduto, 7,8 di finanziamenti agevolati e per il resto l’acquisizione di una partecipazione pubblica al 30% nel capitale dell’azienda. Era un investimento strategico, dissero. Usava l’adenovirus di un gorilla.
Ma il vaccino ReiThera era finito in un cul de sac quasi subito dopo aver terminato la fase1: 45 volontari tra i 18 e i 55 anni e altrettanti tra i 65 e gli 85. Era quindi andato per tre settimane in sperimentazione in fase2: 900 volontari in 21 centri italiani e uno in Germania, fase che doveva terminare a fine maggio 2021. Dopodiché doveva iniziare la fase tre, con migliaia di volontari: al che era evidente che era sperimentale.
Stando ai comunicati itituzionali diramati a piene mani anche dall'Ansa , il vaccino usava una tecnica classica ed era stato sviluppato dalla società biotecnologica di Castel Romano e dall’Istituto per le malattie infettive Spallanzani di Roma.
L’obiettivo (citiamo sempre da quei comunicati) era: ''....arrivare tra settembre ed ottobre 2021 a chiedere all’Ema l’autorizzazione all’utilizzo''.
Ma sul mercato c'era già Pfizer e la scommessa di produrre il siero senza avere la certezza che fosse poi approvato dall’Ema deve aver scoraggiato qualcuno. La scelta dell’Europa metteva fuori gioco i vaccini a vettore virale. Esperti dissero che i danni dei vaccini a vettore virale (rari casi di trombosi in soggetti con poche piastrine) si vedono subito. Altri obiettarono che quelli dei sieri a RNA messaggero potevano sorgere nel lungo periodo con il rischio di mutazioni a lungo termine nel DNA.
Cosa puntualmente accaduta.
www.giornalesentire.it - riproduzione riservata*






















Commenti (0)
Per lasciare un commento